Nat Commun:基因编辑疗法有望高效治疗莱伯氏遗传性视神经病变
来源:生物谷原创 2026-02-23 12:55
这是世界上首个在活体线粒体疾病模型中证明基因编辑治疗效力的研究,为长期缺乏有效治疗手段的患者带来了新的可能性和希望。
研究团队首次在世界上成功展示了针对莱伯氏遗传性视神经病变(LHON)的基因编辑治疗方法。该研究由首尔大学兽医学院与Edgene Co., Ltd.合作完成。此项研究成果以“活体线粒体碱基编辑恢复LHON小鼠模型的基因型与视觉功能”为题,发表在《Nature Communications》期刊上。

LHON是一种母系遗传的线粒体疾病,因视神经细胞退化导致中心视力快速丧失并最终失明。该病好发于十几岁至三十多岁的青年男性,被全球公认为主要的遗传性视神经病变,估计全世界约有30,000至50,000名患者。
LHON由线粒体DNA复合物I基因(如MT-ND4、ND1和ND6)的点突变引起。其中,MT-ND4基因的m.G11778A突变约占全部病例的70%。然而,由于传统CRISPR基因编辑系统使用的向导RNA无法穿透线粒体,基因疗法长期以来被认为不可行。
目前唯一获批的药物艾地苯醌仅能为线粒体功能提供有限的暂时性支持,无法带来根本性的治疗益处。因此,开发精确的疾病模型和根治性基因矫正技术已成为全球紧迫的优先事项。
研究团队利用高保真线粒体碱基编辑平台(Hifi-DdCBE),成功在小鼠中构建了MT-ND4 G11778A等价突变(m.G11185A)。由此产生的小鼠模型忠实地再现了人类LHON的关键病理特征,包括视网膜神经节细胞层变薄、神经节细胞数量减少和视觉功能受损。
随后,团队采用了2024年发表于《Cell》期刊的、经精准增强的TALE连接脱氨酶(TALED-V28R)治疗策略,并通过腺相关病毒载体进行递送。玻璃体内注射AAV-TALED-V28R成功矫正了视网膜神经节细胞中的致病性线粒体DNA突变。视网膜厚度和视网膜神经节细胞计数均恢复到正常水平,通过视动性眼震和视网膜电图评估的视觉功能也显示出显著改善。此外,将TALED-V28R应用于患者来源的细胞后,ATP生成和线粒体复合物I活性得以恢复,进一步支持了其临床转化潜力。
共同第一作者、博士生Sanghun Kim表示:“这项研究为长期缺乏有效治疗手段的患者带来了新的可能性和希望。”他补充道:“我们将继续推进线粒体基因编辑技术,迈向实际临床应用。”
共同首席研究员、资深通讯作者Hyunji Lee教授强调:“这是世界上首个在活体线粒体疾病模型中证明基因编辑治疗效力的研究。”她进一步表示:“我们希望针对包括LHON在内的线粒体疾病的基因编辑疗法能够推进到临床应用阶段,并最终成为可商业化提供的治疗手段。”(生物谷Bioon.com)
参考文献:
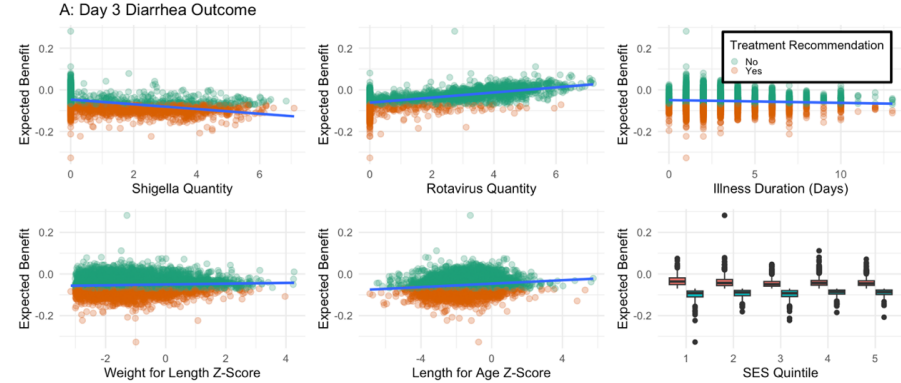
Sara S. Kim et al, Personalized azithromycin treatment rules for children with watery diarrhea using machine learning, Nature Communications (2025). DOI: 10.1038/s41467-025-60682-9.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


 NGS
NGS 引物与探针
引物与探针 RNA合成
RNA合成 基因合成
基因合成 寡核苷酸池
寡核苷酸池 CRISPR sgRNA定制文库
CRISPR sgRNA定制文库 抗体库
抗体库 突变体库
突变体库




 电话:400-800-8820
电话:400-800-8820 地址:苏州市高新区88号
地址:苏州市高新区88号 邮箱:
邮箱: 电话:400-800-8820
电话:400-800-8820 地址:苏州市高新区88号
地址:苏州市高新区88号 邮箱:
邮箱:







